人类认识镁元素的历程可以追溯到1755年,当时英国的josephblack首次确认了镁是一种元素。然而,直到1792年,antonrupprecht才首次通过加热苦土和木炭的混合物制取出不纯净的镁金属。1808年,英国化学家sirhumphrydavy电解汞和氧化镁的混合物,得到镁汞齐,将镁汞齐中的汞蒸馏后,就得到了银白色的金属镁。然而,由于镁的化学性质活泼,难以保存,因此并没有得到广泛的应用。
直到19世纪中叶,随着钢铁工业的发展,人们开始广泛使用镁合金来生产轻便的飞机部件等,使得镁得到了更为广泛的应用。然而,当时人们普遍认为镁只是一种罕见的化学元素,对人体的意义并不大。
直到1934年,麦科勒姆(ElmerVernerMcCollum)通过实验观察到狗和老鼠缺乏镁会导致明显的生长发育异常,自此,人们才开始认识到镁元素的生物学重要性。此后,科学家对镁营养素的研究逐渐深入,越来越多的研究发现镁与骨骼、心血管系统和精神健康等众多方面的密切关联。
现在,我们已经知道,镁是一种人体必需的微量元素,它参与了人体许多重要的生物化学反应。同时,镁也是许多酶的关键组成部分,对于维持人体正常的生理功能至关重要。虽然我们现在对镁的认识已经有了很大的提高,但是关于镁的研究仍然在不断深入,以更好地了解其在人体中的作用和意义。
在我们的日常生活中,无论是在大自然的壮丽景色中,还是在人类的科技进步中,我们都可以看到一种神秘而重要的元素——镁。这种轻飘飘的金属元素,虽然身体微小,但其影响力却无处不在,从生物体的生长发育,到地球的自然循环,再到高科技产品的运行,镁元素都发挥着关键作用。今天,让我们一起深入探索镁的世界,揭示它的魅力和重要性。

镁是一种轻金属元素,具有较低的密度和良好的机械性能。它在许多不同的应用领域中都有广泛的应用,下面是一些镁元素的常见应用领域的详细介绍:
1.汽车工业:镁合金广泛用于汽车制造,包括车身部件、发动机零件、底盘与悬挂系统等。镁合金具有高强度和优异的耐腐蚀性能,可以减轻车身重量,提高燃油效率,并增加车辆的安全性能。
2.航空航天工业:由于其轻量化和高强度特性,镁合金被广泛用于航空航天器件和结构,如飞机发动机零件、飞机座椅、机身结构等。
3.电子产品:镁合金在电子产品中的应用越来越广泛,如手机壳、平板电脑、笔记本电脑外壳等。镁合金具有良好的散热性能和抗电磁干扰能力,可以有效保护电子设备。
4.医疗器械:镁合金在医疗器械领域中也有应用,如人工骨、牙科种植体等。镁合金具有生物相容性,在人体内融合良好,可以促进骨细胞生长和修复。
5.环保领域:镁合金可以用于环保领域的应用,如废水处理、气体净化等。镁合金可以吸附和分解污染物,同时具有再生利用的优势。
镁元素及其合金在许多不同领域都有广泛的应用,主要由于其轻量化、高强度、耐腐蚀和生物相容性等特性。随着技术的进步,预计镁合金的应用领域还将进一步扩大。

镁是一种化学元素,其原子序数为12,在元素周期表中位于第2周期的第2组。以下是镁元素的一些物理性质的详细介绍:
1.密度:镁的密度为1.738g/cm³,是常见金属中相对较低的。这使得镁成为轻量化应用的理想选择,如汽车和航空航天领域。
2.熔点和沸点:镁的熔点为650°C(1,202°F),沸点为1,090°C(1,994°F)。镁具有相对较低的熔点和沸点,这意味着它可以在相对较低的温度下熔融和蒸发。
3.导电性:镁是良好的导电体,具有高电导率。在室温下,镁的电阻率约为43.9nΩ·m,这使得它在电子设备和电气工程中有广泛的应用。
4.磁性:镁是一种顺磁性材料,即在外磁场作用下,它会产生一个与所加磁场方向相同的磁矩。
5.颜色:纯镁是银白色的,具有金属光泽。然而,当镁与空气或水反应时,会形成一层氧化物薄膜,导致其表面出现一种灰色的外观。
6.结晶结构:镁的晶体结构是紧密堆积的六方最密堆积(hcp)。这意味着镁原子在晶体结构中密集排列,具有特定的排列顺序。
7.热传导性:镁具有良好的热传导性能。它的热导率约为156W/(m·K),这使得镁在高温应用和散热领域具有重要作用。
镁元素具有较低的密度、相对较低的熔点和沸点,良好的导电性、磁性和热传导性能,以及银白色的外观。这些物理性质使得镁在许多不同领域有广泛的应用。
镁的化学性质主要涉及其与其他元素或化合物的反应性。以下是镁的一些重要的化学性质:
1.反应性:镁是一种活泼的金属,很容易与非金属元素发生化学反应。例如,镁可以与氧气反应形成氧化镁。镁还可以与酸反应产生氢气。此外,镁还可以与许多其他元素和化合物进行反应,如碳、硫、氮等。
2.氧化性:镁是一种还原剂,具有较高的还原能力。它能够将许多金属氧化物还原为纯金属。例如,镁可以将镁氧化物还原为镁,并将氧气释放出来。
3.酸碱性:镁是一种碱金属,在水中会发生放热的反应。当镁与水反应时,会生成氢氧化镁(Mg(OH)2)和氢气。
4.锌合金化学性质:镁与锌相似,可以形成各种合金。合金化可以改善镁的机械性能和耐腐蚀性。例如,镁铝合金在航空和汽车行业中广泛使用。
5.非金属反应:镁可以与非金属元素如氮、硫、碘等反应。例如,镁可以与氮气反应形成镁氮化物(Mg3N2),与硫反应形成硫化镁(MgS)。
6.酸反应:镁可以与酸发生化学反应,生成相应的盐和氢气。例如,镁与盐酸反应会生成氯化镁和氢气。
镁是一种活泼的金属,具有较高的还原能力。它能够与许多元素和化合物发生化学反应,包括氧气、非金属元素、酸等。镁还可以形成各种合金,提高其机械性能和耐腐蚀性。

镁是一种重要的生物元素,它在生物体中起着多种重要的生理功能。
1.镁对生物体的骨骼和牙齿有着重要的结构支持作用。镁是骨骼和牙齿中的重要成分之一,它可以与钙结合形成稳定的矿物质晶体。这些矿物质晶体赋予了骨骼和牙齿强度和硬度,维持了它们的结构完整性。
2.镁参与细胞能量代谢。镁是细胞内ATP(三磷酸腺苷)的活化剂,可以促进ATP的合成和释放。ATP是细胞内的主要能量储备,细胞需要通过合成和分解ATP来进行各种生物化学反应和能量转换。镁的存在可以提供所需的能量,在细胞能量代谢中起着重要的作用。
3.镁调节神经和肌肉功能。镁离子在神经和肌肉系统中起着重要的调节作用。它可以影响神经传递过程中的离子通道活性和神经递质的释放。此外,镁还可以与肌纤维蛋白相互作用,调节肌肉收缩和松弛。
4.镁参与酶活性。许多酶都需要镁离子的存在来促进酶催化反应。镁离子可以与酶底物结合,促使酶底物产生适当的构象和电荷分布,从而增加酶催化效率和速率。
镁是生物体中一种不可或缺的元素,它在骨骼和牙齿的结构支持、细胞能量代谢、神经肌肉功能和酶活性等方面起着重要的生理功能。

镁是地壳中十分常见的元素,它是地球上第八丰富的元素之一。在地壳中的含量约为2.09%,居于第7位。镁主要以氧化镁(MgO)的形式存在于岩石、矿物和土壤中。
镁的分布具有一定的地域差异。镁丰富的地区主要包括海洋、沉积盆地、火山岩和镁镁橄榄岩等地质环境。海水中的镁离子浓度相对较高,每升海水中含有约1280mg的镁离子。海洋沉积物中也含有大量的镁化合物,如镁镁橄榄石矿物。此外,在一些火山岩和玄武岩中也含有丰富的镁元素。
然而,镁在陆地上的分布相对较少。一般来说,镁的流动性较大,容易被水溶解并随水流迁移,因此在陆地上的相对含量较低。土壤中的镁含量通常比较低,尤其是在经过长期冲刷和淋洗的地区。但是,在某些特殊的地质环境下,如镁贫瘠的岩石和土壤中,可以出现镁的局部富集。
镁在地球上广泛分布,尤其是在海洋和一些特殊的地质环境中存在丰富。在陆地上的相对含量较低,但也在少数地区出现镁的富集现象。

镁元素的开采和提炼过程通常包括以下步骤:
1.开采:镁主要从镁矿中开采。镁矿石通常以死海盐、菱镁矿(MgCO3)、菱镁矾(MgSO4·7H2O)和濛东镁矿(Mg3Si2O5(OH)4)等形式存在。其中,菱镁矿是最常见的镁矿石。开采过程包括地质勘探、爆破、采矿和运输等。
2.矿石破碎和选矿:开采得到的镁矿石需要经过破碎和选矿处理,将其分离出含有较高镁含量的部分。这可以通过机械破碎和浮选等方法实现。
3.提炼:提炼镁元素的主要方法有两种:热法和电解法。
-热法提炼:这是一种常见的镁元素提炼方法。首先,将镁矿石经过破碎和磨粉处理,得到细粉末。然后,使用高温炉将细粉末与还原剂(如铝粉)反应,产生镁蒸气。镁蒸气会在高温下凝结成为固体的镁,然后通过冷却和净化等步骤得到纯度较高的镁金属。
-电解法提炼:这是一种主要用于海水镁的提炼方法。首先,将海水经过浓缩和处理,得到含有镁离子的溶液。然后,将该溶液置于电解槽中,在电流刺激下,镁离子在阴阳极之间发生氧化还原反应,最终得到纯度较高的镁金属。
4.精炼和加工:提炼出来的镁金属通常需要进行进一步的精炼和加工,以提高其纯度和符合特定的应用需求。这可能包括熔炼、再结晶、滚轧和加工成型等工艺。

镁元素的常用检测方法包括以下几种:
原子吸收光谱法(AAS):原子吸收光谱法是一种常用的定量分析方法,利用特定波长的吸收光谱来测定样品中镁元素的浓度。它在火焰中将待测样品原子化,然后通过光谱仪器测量样品中镁元素的吸收强度。该方法适用于较高浓度的镁检测。
电感耦合等离子体发射光谱法(ICP-OES):电感耦合等离子体发射光谱法是一种高灵敏度和高选择性的分析方法,广泛用于多元素分析。它通过将样品雾化并形成等离子体,在光谱仪器中测定镁元素发射的特定波长和强度。
电感耦合等离子体质谱法(ICP-MS):电感耦合等离子体质谱法是一种高灵敏度和高分辨率的分析方法,可用于同位素比值测定和微量元素分析。它通过将样品雾化并形成等离子体,在质谱仪器中测定镁元素的质量荷比值。
X射线荧光光谱法(XRF):X射线荧光光谱法利用样品受到X射线激发后产生的荧光光谱来分析元素的含量。它可以快速、非破坏性地测定样品中的镁元素含量。
分光光度法:该方法利用带有特定试剂的比色剂与镁离子反应生成有色化合物,根据生成的有色化合物的吸光度或颜色深浅来确定镁元素的含量。
直读光谱法:也称为光电直读光谱法,是一种用于分析样品中元素含量的分析技术。直读光谱法基于原子发射光谱分析法的原理。它通过使用高温电火花或电弧将样品中的元素从固态直接气化,并在激发状态下发射出特征谱线。每个元素都有独特的发射谱线,其强度与样品中该元素的含量成正比关系。通过测量这些特征光谱线的强度,可以确定样品中各元素的含量。该方法主要用于金属和合金的成分分析,特别是在冶金、金属加工、材料科学等领域应用广泛。
滴定法:滴定法基于滴定试剂和待测溶液之间的化学反应。通常,滴定试剂是一种已知浓度的化学试剂,可以与待测溶液中的金属离子发生反应,达到反应终点,从而确定金属离子的浓度。滴定过程通常涉及使用指示剂,以便观察到反应的终点。滴定法可以应用于许多不同的金属元素,通常需要选择适当的滴定试剂和指示剂,以确保准确的测量。不同的金属元素可能需要不同的反应条件和指示剂来实现准确的滴定。这种方法广泛应用于化学分析、环境监测、食品分析和质量控制等领域。
这些方法在实验室和工业领域被广泛应用于镁元素的定量分析和质量控制。选择合适的方法取决于样品类型、要求的检测限和检测精度等因素。

在元素测量中,原子吸收法具有较高的准确性和灵敏度,为研究元素的化学性质、化合物组成以及含量提供了有效的手段。
接下来,我们使用原子吸收法来测量镁元素的含量。具体的步骤如下:
制备待测样品。将需要测量的样品制备成溶液,一般需要使用混酸进行消解,以便于后续的测量。
选择合适的原子吸收光谱仪。根据待测样品的性质和需要测量的镁元素含量范围,选择合适的原子吸收光谱仪。
调整原子吸收光谱仪的参数。根据待测元素和仪器型号,调整原子吸收光谱仪的参数,包括光源、原子化器、检测器等。
测量镁元素的吸光度。将待测样品放入原子化器中,通过光源发射特定波长的光辐射,待测镁元素会吸收这些光辐射,产生能级跃迁。通过检测器测量镁元素的吸光度。
计算镁元素的含量。根据吸光度和标准曲线,计算出镁元素的含量。
以下是一款仪器测量镁元素用到的具体参数。
镁(Mg)
标准物:金属镁片或镁丝(99.99%)。
方法:准确称取1.000g金属镁,溶于少量(1+4)HNO3中,用水准确定容至1L,此溶液Mg的浓度为1000μg/mL。避光保存于聚乙烯瓶中。或直接购买带有国家标准物质证书的标准溶液。
火焰类型:空气-乙炔,贫燃焰。
分析参数:
波长(nm)285.2
光谱带宽(nm)0.4
滤波系数0.3
空心阴极灯推荐灯电流(mA)2
负高压(v)245.75
燃烧头高度(mm)6
积分时间(S)3
空气压力及流量(MPa,mL/min)0.22
乙炔压力及流量(MPa,mL/min)0.05,1500
线性范围(μg/mL)0.003~0.4
线性相关系数0.9991
特征浓度(μg/mL)0.005
检出限(μg/mL)0.001
RSD(%)0.49
计算方式连续法
溶液酸度0.5%HNO3
测量表格:
序号
测量对象
样品编号
Abs
浓度
SD
RSD[%]
1
标准样品
Mg1
-0.001
0.000
0.0003
-43.8479
2
标准样品
Mg2
0.099
0.100
0.0005
0.4793
3
标准样品
Mg3
0.196
0.200
0.0004
0.1941
4
标准样品
Mg4
0.294
0.300
0.0014
0.4867
5
标准样品
Mg5
0.373
0.400
0.0009
0.2298
校准曲线:
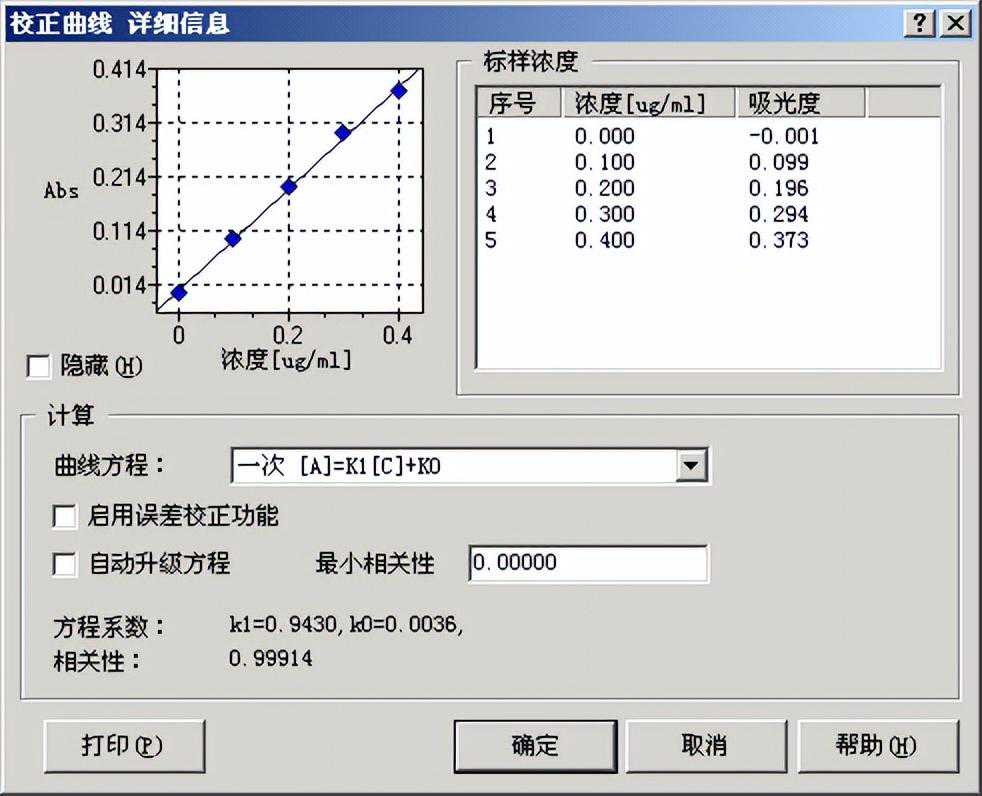
干扰:
在空气-乙炔火焰中最常见的干扰可以加入“释放剂”克服,最常使用的释放剂是Sr(1000~5000μg/mL)或La(10000μg/mL)。
酸度对测定有影响,故应控制标准溶液和样品的酸度一致。
Mg是最灵敏的元素之一,应严格控制水和试剂的空白,避免试剂、容器、实验室灰尘的污染。
实际工作中需要根据现场具体需要选择适合的测量方法。这些方法在实验室和工业中广泛应用于镁元素的分析和检测。
镁元素,这个看似平凡的金属元素,却拥有着非凡的特性和应用。从航空航天到生物医学,从电子科技到环保能源,镁元素在各个领域都发挥着至关重要的作用。它既是一种轻质、高强度的金属,又是一种人体必需的微量元素,更是许多领域的关键材料。在这个充满无限可能的时代,让我们继续探索镁元素的更多奥秘,为人类的未来创造更美好的明天。